在2024年,基因和细胞疗法仍然是第一个市场中最热门的投资轨道。
超过50亿美元倒入
在2024年仍然相对静默的医疗和健康市场中,基因和细胞疗法轨道非常活跃,它们更令人眼花azz乱。
根据动脉橙色数据库的数据,2024年,全球共有157家遗传和细胞治疗公司完成了171个融资,累计筹集资金超过51.9亿美元。根据2024年的“ 2024年全球投资和金融分析报告”,在2024年,基因和细胞疗法领域是整个医疗和健康行业中总融资最大且交易活动最高的地区。
但是,如果将观察的观点深入到2024年,那么在国内外,基因和细胞疗法融资就已经显着开放。从最终融资数据的角度来看,海外市场的遗传和细胞疗法融资是该细分市场增长的更重要差距。
首先,就节奏融资而言,海外的第一级市场基因以及细胞疗法投资和融资交易更加活跃。在中国,2024年,共有70家基因和细胞治疗公司完成了75份融资交易,涉及超过8.1亿美元。其中,Laimang Biological全年进行了三轮公共融资,累计筹款超过2000万美元; Yue种族生物,引用的基因,信仰级别的医学和Rongze集团已经完成了两轮融资。
相对而言,2024年遗传和细胞疗法公司的融资状况更加受欢迎。全年总共完成了88家公司完成96家融资交易。其中,Hephaistos-Pharma全年公开筹集了三轮,总计超过1200万美元; Vico Therapeutics,Santa Ana Bio,Neurona Therapeutics,Neurenati Therapeutics和Indapta Therapeutics以及Brenus Pharma和其他6家公司已经完成了两轮融资。
第二个是融资金额。由于在2024年获得融资的海外基因和细胞治疗公司,其中大多数是企业家中期和晚期的成熟项目,相应的融资金额也更高。 2024年9月,总部位于加利福尼亚的细胞疗法公司阿森纳生物宣布完成了3.25亿美元的C系列融资,这是当年的遗传和细胞公司最高数量。这也是该曲目中唯一的一个。医疗和卫生融资的十大交易。在中国,2024年4月,基于信件的药品制药药医学是上海的总部,宣布完成了3500万美元的票房,成为一年中家庭和细胞疗法领域中最高的融资。在一轮融资阶段,年度最高的融资金额最高,这是从世界上最高的融资中挤出的。
此外,值得注意的是,与纯粹基于基于出色的生物技术能力的企业家项目相比,到2024年,国内和外国资本更喜欢具有明显的临床或技术属性的基因和外国资本。
例如,在赛道年度获得最高融资的阿森纳生物是在物理肿瘤CAR-T领域的明星公司。该公司的两个共同创始人,一个是肝移植外科医生,他从事风险投资,另一位是默克研究实验室的肿瘤学和免疫学副总裁。临床和医疗资源。前面提到的XIN级医学是在2023年在上海Baoshan Xin -Level Medicine建立的。作为上海生物学研究所直接相关的单位,XIN -Level Medicine依赖于上海生物学研究所和Zhejiang,Jiangsu,Shanghai和Shanghai和Shanghai和Zhejiang其他地方。医院建立了合作,以开放临床患者的绿色通过,商业发展的优势显而易见。
就技术属性而言,一年赢得三轮融资的Laimang生物具有AI和Biotechnology整合的特征,可以在许多同伴中脱颖而出。 Laimang Biology成立于2021年,由瑞士洛桑联邦技术学院(EPFL)教授唐·李(Tang Li)团队创立。
当然,即使在如此炎热的一年中,基因和细胞疗法领域的资金差距仍然很明显。 2024年,动脉网络的CGT公园走了11个公园。在此过程中,客人提到了融资困境。一项工作说,许多机会应该非常活跃,因为现在没有多少资金可以投资,但是有很多项目缺乏钱。另一位从业者指出,专注于有限管道的有限资源必须具有创新,但只有有限的创新。必须有区别,但实际上很难确定。
02商业化爆发
在2024年,在第一个级别市场的火热融资背后,在密集的遗传和细胞疗法产品中取得了重要的进展。这项突破性的生物治疗计划为许多主要的人类疾病提供了唯一的解决方案。根据动脉橙色数据库的不完整统计数据,2024年,全球共有18种基因和细胞治疗产品被批准列出,远远超过了2023年的水平。更重要的是,有许多新的新药物。
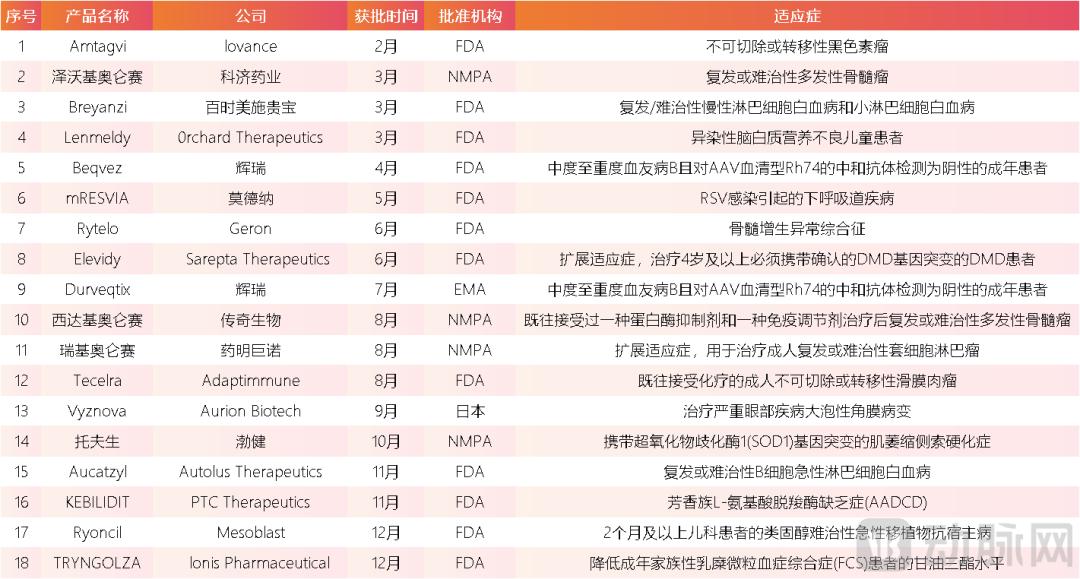
在2024年,批准了第一种新药将遗传和细胞治疗临床应用的边界列为更多疾病。 2月16日,IOVANCE的Amtagvi(Lifileucel)获得了美国FDA的批准,成为世界上第一种肿瘤浸润淋巴细胞疗法,用于治疗非脱毛或转移性黑色素瘤。在此之前,大多数非灭绝或转移性黑色素瘤的患者主要通过靶向疗法或传统的镶嵌化疗来扩展。在国际多中心II的II期临床试验中,Amtagvi单药治疗是非经过改革或转移性黑色素瘤的,并且客观缓解率达到31.4%,其中包括8例完全缓解的病例和40例病例。预后。
3月14日,Beltay Squibb的Breyanzi获得了FDA的批准,FDA用于治疗复发/难治性慢性淋巴细胞白血病或小淋巴细胞淋巴瘤成年患者,其上市价格为410,300美元。这也是世界上第一种批准治疗复发或治愈慢性淋巴细胞白血病或小淋巴细胞淋巴瘤的CAR-T细胞疗法。在关键的多中心测试超越CLL004中,完整的缓解率为20%,总救济率为45%。在已经完全缓解的患者中,没有实现培养基救济的持续时间,血液中小残留疾病的负率为100%,骨髓为92.3%。
此外,值得一提的是,2024年8月,全球第一种TCR-T疗法被批准用于上市。这种名为Tecelra的TCR-T产品是由Adaptimmune开发的,并获得FDA批准以治疗以前接受化疗的成年人。与CAR-T相比,TCR-T治疗一直被认为是一种更先进的细胞疗法溶液,但商业化非常慢。 Tecelra的批准无疑极大地激发了TCR-T领域的发展和投资热情。
根据动脉橙数据库的统计,截至2024年底,全球已批准了50多种基因和细胞疗法药物。但是,从上市后的商业性能的角度来看,这首曲目无疑是从距离距离远处的很长的路要走。
从2024年宣布的商业数据的角度来看,除了Sidaki Olun Sai注入液体外,大多数基因和细胞疗法恒星产品仍然不理想。数据显示,2024年,Sidaki Olun Saitar的注射量为9.63亿美元,增长了92.7%,而不是2023年。Kymriah,Abecma等。2024年,销售额的销售额缩水到不同程度。
一方面,大量新产品被批准被密集列出,另一方面,临床应用的普及相对较慢,并且基因和细胞疗法的商业化近战似乎是不可避免的。数据表明,自上市以来,两种国内细胞疗法产品Rocky Olun和Zerokiolon并没有带来突破性的收入贡献。数据表明,在2024年上半年,洛基·奥伦(Rocky Olun)的注射收入贡献了8681.5亿元,而扎夫沃基·奥伦(Zavvoki Olun)售出了约600万元。
03什么时候出现商业化点?
到2025年,随着越来越多的企业和研究机构进入,研究管道和临床试验的数量继续增加,产品均匀性的均匀性逐渐出现,遗传和细胞疗法的商业化可能落入红海。争议。但是,始终需要解决这种创新疗法的两个主要瓶颈。
一方面,遗传和细胞疗法本身仍然具有更大的安全风险。这也是该技术广泛临床应用的关键瓶颈。例如,存在交付系统的风险。常用的基因疗法AAV载体对肝脏具有高亲和力。它可能引起免疫系统攻击,肝毒性,并可能导致染色的体重增加和降低剂量的风险,甚至引起癌症。另一个例子是编辑工具可能带来的问题,基因编辑工具,例如基因和细胞疗法中常用的CRISPR/CAS9,这实际上正在改变DNA序列。它影响肿瘤抑制基因,带来隐藏的安全危害。
另一方面,成本高且价格昂贵的患者群体有限。正是因为基因和细胞疗法的技术成熟度仍然受到限制,因此这种产品的应用仅限于非常有限的范围,并且管理要求非常严格。以基因疗法为例,病毒载体的产生需要大型工厂。生产过程很复杂,质量控制很困难,导致成本高昂。例如,由于病毒携带者的生产成本高,某些基因治疗产品很昂贵。在现有的技术条件下,基因和细胞疗法的研发需要大量资本,人才和时间投资。从实验室研究到临床试验再到产品上市,该过程很复杂,风险很高。许多创新的制药公司都面临着财务压力和研发的失败。风险,有限的空间可从供应方面降低定价。
在付款方面,这种保证定位与基本医疗保险不符,并且很难通过常规准确性进入国家医疗保险目录。尽管由于过去症状的限制和支付的上限,保护范围,付款的努力和覆盖范围有限,但由于某些商业保险和本地福利包括保证的某些细胞和基因治疗产品范围无法满足患者的需求。
从某种意义上说,遗传和细胞疗法的商业化近战可能比转折点早。但是,随着技术本身的持续改进,为了覆盖更广泛的患者群体,我们认为这种创新疗法将成为诊所中非常重要的治疗工具。
本文来自由36氪发行的微信公共帐户:Wang Shiwei。

